曾经是各种疾病的模糊替罪羊,越来越多的证据表明,一种被称为“肠漏症”的疾病——微生物和其他分子从肠道中渗出——可能比以前认为的更常见,也更有害。
肠漏症最常发生在老年人、癌症或其他慢性病患者以及生活压力特别大的人身上。压力源会破坏形成肠壁的细胞之间的拉链状连接。随后通过这些细胞间隙漏出的微生物和分子会引发免疫反应,导致慢性炎症引起的多种疾病,例如炎症性肠病、痴呆、动脉粥样硬化、肝纤维化、癌症、糖尿病和关节炎。
然而,临床医生并没有很好的方法来判断谁有肠漏,谁没有——而且也没有治疗方法来修复它。
加州大学圣地亚哥分校医学院的研究人员现在能够使用从患者细胞生成的人体肠道 3-D 模型,首次模拟肠漏情况。这些小型类器官或“迷你内脏”揭示了新的生物标志物,这些生物标志物有助于确定肠漏症的外观——分子信号有朝一日可以帮助临床医生更好地诊断病情、跟踪病情进展并评估治疗的成败。该团队还使用该模型探索了一种潜在的途径,可以通过一种常见的可用药物来收紧肠漏症。
该研究于 2020 年 2 月 10 日在生命科学联盟上发表,由第一作者、加州大学圣地亚哥分校医学院和摩尔癌症中心细胞与分子医学教授 Pradipta Ghosh 博士和资深作者 Soumita Das 博士领导., 加州大学圣地亚哥分校医学院病理学副教授。
Ghosh 及其同事此前发现了一种有助于收紧肠壁连接的特殊分子机制——他们将这种机制称为压力极性信号通路。他们发现,当通路受到压力时,连接点会松开。他们还发现糖尿病药物二甲双胍可能有助于激活该通路,收紧连接的迹象。但这些基本发现是在培养皿中培养的细胞系中做出的,与人类无关——至少目前还没有。
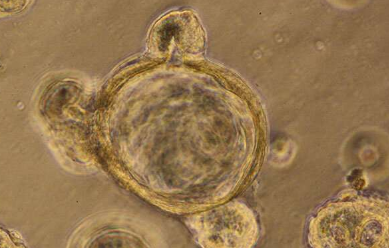
因此,Ghosh、Das 和团队转向了仅次于人类测试对象的最佳选择:来自患者肠道的 3-D 肠道类器官。肠道的内壁并不光滑,更像是崎岖不平的地形,有许多山峰和山谷。在每个被称为地穴的山谷底部,都有小型的干细胞库。为了生产肠道类器官,研究人员从患者活组织检查中收集了少量这些干细胞,并在实验室中培养它们。正如它们在人的肠道中所做的那样,干细胞分化或特化为构成肠道内壁的四种不同细胞类型。但在实验室里,在体外,它们卷成一团,形成了隐窝。换句话说,“迷你胆量”。
 新传媒网
新传媒网